Đề thi giữa kì 2 Hóa học 10 Cánh diều năm 2023 – 2024 bao gồm 2 đề kiểm tra có đáp án giải chi tiết kèm theo đề tự luyện. Thông qua đề kiểm tra giữa kì 2 Hóa học 10 Cánh diều giúp các bạn có thêm nhiều tư liệu học tập, ôn luyện đề tốt hơn.
Bạn đang đọc: Bộ đề thi giữa học kì 2 môn Hóa học 10 năm 2023 – 2024 sách Cánh diều
TOP 2 Đề kiểm tra học kì 2 Hóa học 10 Cánh diều được biên soạn bám sát nội dung chương trình trong sách giáo khoa. Thông qua đề thi Hóa học 10 giữa học kì 2 sẽ giúp quý thầy cô giáo xây dựng đề kiểm tra theo chuẩn kiến thức và kỹ năng, nhanh chóng biên soạn đề thi cho các em học sinh của mình. Ngoài ra các bạn xem thêm: đề thi giữa kì 2 môn Tin học 10 Cánh diều, đề thi giữa kì 2 Toán 10 Cánh diều, đề thi giữa kì 2 môn Ngữ văn 10 Cánh diều.
Bộ đề thi giữa kì 2 môn Hóa học 10 Cánh diều
1. Đề thi giữa kì 2 Hóa 10 Cánh diều – Đề 1
2. Đề thi giữa học kì 2 môn Hóa học 10 – Đề 2
1. Đề thi giữa kì 2 Hóa 10 Cánh diều – Đề 1
1.1 Đề thi giữa kì 2 Hóa 10
Cho nguyên tử khối của các nguyên tố: Mn = 55, O = 16, Mg = 24, Fe=56, H = 1, Ag = 108, K = 39, Cl = 35,5, F = 19, Br = 80, I = 127, S = 32, Zn = 65, Cu = 64, Al = 27.
I. Trắc nghiệm ( 3 điểm)
Câu 1: Phát biểu nào sau đây là sai?
A. Bán kính nguyên tử của clo lớn hơn bán kính nguyên tử của flo.
B. Độ âm điện của brom lớn hơn độ âm điện của iot.
C. Tính khử của ion Br– lớn hơn tính khử của ion Cl–.
D. Tính axit của HF mạnh hơn tính axit của HCl.
Câu 2: Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là
A. Ag, CaCO3, CuO.
B. FeS, BaSO4, KOH.
C. AgNO3, (NH4)2CO3, Cu.
D. Mg(HCO3)2, AgNO3, CuO.
Câu 3: Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách
A. điện phân nóng chảy NaCl.
B. cho dung dịch HCl đặc tác dụng với MnO2, đun nóng.
C. điện phân dung dịch NaCl có màng ngăn.
D. cho F2 đẩy Cl2 ra khỏi dung dịch NaCl.
Câu 4: Cho kim loại M tác dụng với Cl2 được muối X; cho kim loại M tác dụng với dung dịch HCl được muối Y. Nếu cho kim loại M tác dụng với dung dịch muối X ta cũng được muối Y. Kim loại M có thể là
A. Mg.
B. Zn.
C. Al.
D. Fe.
Câu 5: Khi cho dung dịch AgNO3 phản ứng với dung dịch nào sau đây sẽ cho kết tủa màu vàng đậm nhất?
A. Dung dịch HI.
B. Dung dịch HCl.
C. Dung dịch HBr.
D. Dung dịch HF.
Câu 6: Trong phản ứng: Cl2 + H2O ↔ HCl + HClO, clo đóng vai trò
A. không là chất oxi hóa, không là chất khử.
B. là chất oxi hóa.
C. là chất khử.
D. vừa là chất oxi hóa, vừa là chất khử.
Câu 7: Trong phòng thí nghiệm, dung dịch HF không được bảo quản trong bình làm bằng chất liệu nào?
A. Nhựa.
B. Gốm sứ.
C. Thủy tinh.
D. Polime.
Câu 8: Cho 5,4 gam Al phản ứng hoàn toàn với dung dịch HCl loãng, dư thu được bao nhiêu lít khí H2 (đktc)?
A. 4,48 lít.
B. 2,24 lít.
C. 6,72 lít.
D. 7,84 lít.
Câu 9: Cho 0,1 mol KMnO4 tác dụng với dung dịch HCl dư, đun nóng. Thể tích khí thoát ra (ở đktc) là
A. 0,56 lít.
B. 5,6 lít.
C. 2,24 lít.
D. 0,112 lít.
Câu 10: Khi cho mẩu quỳ tím ẩm vào bình đựng khí Cl2, hiện tượng thu được là
A. quỳ tím chuyển sang màu đỏ.
B. quỳ tím không chuyển màu.
C. quỳ tím chuyển sang màu đỏ, sau đó mất màu.
D. quỳ tím chuyển sang màu xanh.
II. Tự luận ( 7 điểm)
Câu 1 ( 2 điểm): Bằng phương pháp hóa học (không dùng chất chỉ thị) hãy phân biệt các dd sau chứa trong các lọ riêng biệt mất nhãn: MgCl2, KBr, KCl.
Câu 2 ( 2 điểm): Cho m gam hỗn hợp G gồm: CaCO3 và Al vào một lượng vừa đủ V lít dung dịch HCl 2M. Sau phản ứng thu được dung dịch A và 8,96 lít khí B ở đktc. Cô cạn A thu được 37,8 gam muối khan.
1/ Xác định % khối lượng của các chất trong G.
2/ Tính CM của các chất trong A.
Câu 3 ( 2 điểm): Cho 5,965 gam hỗn hợp A gồm: NaX, NaY (X,Y là hai halogen liên tiếp, nguyên tử khối của X 3 dư. Kết thúc phản ứng thu được 1,435gam kết tủa. Xác định hai nguyên tố X, Y.
Câu 4 ( 1 điểm): Sục V lít Cl2 ở đktc vào 100ml dung dịch C gồm: NaF 1M; NaBr 3M và KI 2M thu được dung dịch D. Cô cạn D thu được 41,1 gam chất rắn khan E. Xác định V.
1.2 Đáp án đề kiểm tra giữa kì 2 Hóa học 10
I. Trắc nghiệm ( 0,3 điểm/câu)
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đáp án | D | D | B | D | A | D | C | C | B | C |
II. Tự luận ( 7 điểm)
Câu 1 ( 2 điểm):
Đánh số thứ tự từng lọ, trích mẫu thử. (0,5 điểm)
Dùng dd NaOH nhận ra MgCl2 nhờ kết tủa trắng (0,5 điểm)
PTHH: MgCl2 + 2NaOH → Mg(OH)2 (↓) + 2NaCl.
Dùng dd AgNO3 nhận ra KCl (kết tủa trắng), KBr (kết tủa vàng nhạt). (0,5 điểm)
PTHH: (0,5 điểm)
AgNO3 + KCl → AgCl + KNO3
AgNO3 + KBr → AgBr + KNO3.
(viết đúng mỗi PTHH 0,25 điểm)
Câu 2 ( 2 điểm):
1. Gọi số mol CaCO3 = x; số mol Al = y; tính số mol khí = 0,4 mol. (0,25 điểm)
CaCO3 + 2HCl → CaCl2 + CO2 + H2O (0,5 điểm)
x → x (mol)
2Al + 6HCl → 2AlCl3 + 3H2
y → 1,5y (mol)
(mỗi PTHH đúng 0,25 điểm)
Lập hệ: (0,25 điểm)
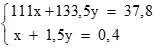
Giải hệ: x = 0,1; y = 0,2
Tính được %mCaCO3 = 64,935%; %mAl = 35,065%.
2. Tính số mol HCl pư = 0,8 mol và tính V = 0,4 lít. (0,25 điểm)
Tính số mol các chất tan trong A: CaCl2 0,1 mol và AlCl3 = 0,2 mol. (0,25 điểm)
Tính được: CMCaCl2 = 0,1:0,4 = 0,25M; CMAlCl3 = 0,2:0,4 = 0,5M. (0,25 điểm)
Câu 3 ( 2 điểm):
Trường hợp 1: X là Flo và Y là Clo. Ta có PTHH: (0,25 điểm)
Tính được số mol AgCl = 0,01 mol
NaCl + AgNO3 → AgCl + NaNO3 (0,5 điểm)
0,01 ← 0,01 (mol)
→ mNaCl = 0,01.58,5 = 0,585
Trường hợp 2: X khác F gọi X, Y là E (điều kiện: 35,5 E
NaE + AgNO3 → AgE + NaNO3
Ta có số mol NaE = số mol AgE (0,5 điểm)
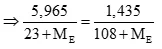
Giải PT → ME
Câu 4 ( 1 điểm):
Các pư có thể xảy ra theo thứ tự: (0,25 điểm)
Cl2 + 2KI → 2KCl + I2 (1)
0,1← 0,2 → 0,2 (mol)
Cl2 + 2NaBr → 2NaCl + Br2 (2)
0,3 → 0,3 (mol)
npư: x → 2x → 2x (mol)
Số mol các chất: NaF 0,1 mol; NaBr 0,3 mol; KI 0,2 mol
– Giả sử Cl2 phản ứng vừa đủ ở phản ứng 1. (0,25 điểm)
Theo pư 1: Chất rắn E gồm: NaF 0,1 mol; KCl 0,2 mol; NaBr 0,3 mol
m1 = 0,1.42 + 0,2.74,5 + 0,3.103 = 50 gam.
– Giả sử Cl2 phản ứng vừa đủ ở phản ứng 2. (0,25 điểm)
Theo phản ứng 1,2: Chất rắn E gồm: NaF 0,1 mol; KCl 0,2 mol; NaCl 0,3 mol
m2 = 0,1.42 + 0,2.74,5 + 0,3.58,5 = 36,65 gam.
Nhận xét: m2E 1 → Pư 2 mới xảy ra 1 phần
Gọi số mol Cl2 pư ở 2 là x mol: Theo pư 1,2: (0,25 điểm)
– E gồm: NaF 0,1 mol; KCl 0,2 mol; NaCl 2x mol; NaBr (0,3-2x) mol
Ptr: 0,1.42 + 0,2.74,5 + 2x.58,5 + (0,3-2x).103 = 41,1 x = 0,1
– Số mol Cl2 đã dùng = 0,1+x = 0,2 mol → V = 0,2.22,4 = 4,48 lít
2. Đề thi giữa học kì 2 môn Hóa học 10 – Đề 2
Họ và tên học sinh:…………………………………… SBD:………………………….
Cho nguyên tử khối của các nguyên tố: H=1; C=12; O=16; Na=23; Mg=24; Al=27; S = 32;
Cl =35,5; K=39; Fe=56; Ba=137.
I. PHẦN TRẮC NGHIỆM: (7,0 điểm)
Câu 1: Trong phòng thí nghiệm, điều chế hiđro clorua bằng cách cho H2SO4 đặc vào ống nghiệm chứa chất rắn X rồi đun nóng. Chất X là
A. Cu.
B. NaCl.
C. NaOH.
D. Cu(OH)2.
Câu 2: Chất hoặc dung dịch nào sau đây không phản ứng với Cl2?
A. NaI.
B. O2.
C. CaBr2.
D. H2.
Câu 3: Cl2 thể hiện đồng thời tính oxi hóa và tính khử trong phản ứng với
A. Fe.
B. NaI.
C. H2.
D. H2O.
Câu 4: Ở điều kiện thường, clo là chất
A. rắn màu vàng.
B. khí không màu.
C. khí màu vàng lục.
D. rắn màu lục nhạt.
Câu 5: Axit HCl tác dụng với CuO tạo ra sản phẩm gồm những chất nào sau đây?
A. CuCl2, H2O.
B. CuCl2, H2.
C. Cu, H2O.
D. Cu, H2.
Câu 6: Clorua vôi là muối của canxi với 2 loại gốc axit là clorua (Cl- )và hipoclorit (ClO-). Vậy Clorua vôi gọi là muối gì?
A. Muối hỗn tạp.
B. Muối của 2 axit.
C. Muối trung hoà.
D. Muối kép.
Câu 7: Các dung dịch: NaF, NaI, NaCl, NaBr. Chỉ dùng một thuốc thử nào sau đây để nhận biết các dung dịch trên?
A. Cl2. B.
Dung dịch AgNO3.
C. Hồ tinh bột.
D. Dung dịch NaOH.
………..
Tải file tài liệu để xem thêm đề thi giữa kì 2 Hóa học 10
