Hóa 12 Bài 9 giúp các em học sinh nắm vững được kiến thức về tính chất vật lý và trạng thái tự nhiên, cấu trúc phân tử của Amin. Đồng thời giải nhanh được các bài tập Hóa 12 chương 1 trang 44.
Bạn đang đọc: Hóa học 12 Bài 9: Amin
Giải bài tập Hóa 12 bài 9 trước khi đến lớp các em nhanh chóng nắm vững kiến thức hôm sau ở trên lớp sẽ học gì, hiểu sơ qua về nội dung học. Đồng thời giúp thầy cô tham khảo, nhanh chóng soạn giáo án cho học sinh của mình. Vậy sau đây là nội dung chi tiết tài liệu, mời các bạn lớp 12 cùng tham khảo tại đây.
Giải Hóa 12 bài 9 Amin trang 44
Lý thuyết Hóa 12 bài 9 Amin
I. Khái niệm, phân loại và danh pháp
1. Khái niệm, phân loại
Khi thay thế nguyên tử H trong phân tử NH3 bằng gốc hiđrocacbon ta thu được amin.
Thí dụ:
NH3: amoniac
CH3NH2: metylamin
C6H5NH2: phenylamin
Amin thường có đồng phân về mạch cacbon, về vị trí của nhóm chức và về bậc amin.
Thí dụ: Viết đồng phân của hợp chất có công thức phân tử: C3H9N
CH3-CH2-CH2-NH2: propan-1-amin
CH3-CH2-NH-CH3: N-metyl-etan-1-amin
CH3-CH(CH3)-NH2: propan-2-amin
(CH3)3-N: trimetyl amin
Amin được phân loại theo hai cách thông dụng nhất:
a) Theo gốc hiđrocacbon
* Amin mạch hở như CH3NH2, C2H5NH2,…,
* Amin thơm như C6H5NH2, CH3C6H4NH2,…
b) Theo bậc của amin (Bậc amin thường được tính bằng số gốc hiđrocacbon liên kết với nguyên tử nitơ):
* Amin bậc một như C2H5NH2
* Amin bậc hai như CH3-NH-CH3
Amin bậc ba như (CH3)3-N
2. Danh pháp
Tên của các amin thường được gọi theo tên gốc – chức (gốc hiđrocacbon với chức amin) và tên thay thế.
Tên của một vài amin
| Công thức cấu tạo | Tên gốc – chức | Tên thay thế |
| CH3NH2 | metylamin | metanamin |
| CH3CH2NH2 | etylamin | etanamin |
| CH3NHCH3 | đimetylamin | N-metylmetanamin |
| CH3CH2CH2NH2 | propylamin | propan-1-amin |
| (CH3)3N | trmetylamin | N, N – đimetylmetanamin |
| CH3[CH2]3NH2 | butylamin | butan – 1- amin |
| C2H5NHC2H5 | đietylamin | N-etyletanamin |
| C6H5NH2 | phenylamin | benzenamin |
| H2N[CH2]6NH2 | hexametylenđiamin | hexan-1,6-điamin |
II. Tính chất vật lí
Metylamin, đimetylamin, trimetylamin và etylamin là những chất khí, mùi khai khó chịu, tan nhiều trong nước.
Các amin có phân tử khối cao hơn là những chất lỏng hoặc rắn, nhiệt độ sôi tăng dần và độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
Các amin thơm là chất lỏng hoặc chất rắn và dễ bị oxi hóa.
Các amin đều độc.
III. Cấu tạo phân tử và tính chất hóa học
1. Cấu tạo phân tử
Trong phân tử amin, nguyên tử N tạo được một, hai hoặc ba liên kết với gốc hiđrocacbon, tương ứng có amin bậc một RNH2, amin bậc hai R-NH-R1, amin bậc ba:
Như vậy, phân tử amin có nguyên tử nitơ tương tự như trong phân tử NH3 nên các amin có tính bazơ. Ngoài ra, amin còn có tính chất của gốc hiđrocacbon.
2. Tính chất hóa học
a) Tính bazơ
* Thí nghiệm 1
Nhúng giấy quỳ tím vào dung dịch metylamin hoặc propylamin, màu quỳ tím chuyển thành xanh. Nếu nhúng quỳ tím vào dung dịch anilin, màu quỳ tím không đổi.
Giải thích:
Metylamin và propylamin cũng như nhiều amin khác khi tan trong nước phản ứng với nước tương tự NH3, sinh ra ion OH-.
CH3NH2 + H2O ⇔ [CH3NH2]+ + OH–
Thí dụ:
Anilin và các amin thơm khác phản ứng rất kém với nước.
Giải bài tập Hóa 12 bài 9 trang 44
Câu 1
Có 3 hóa chất sau đây: Etylamin, phenylamin, amoniac. Thứ tự tăng dần tính bazơ được xếp theo dãy:
A. Amoniac
B. Etylamin
C. Phenylamin
D. Phenylamin
Gợi ý đáp án
Đáp án C.
Câu 2
Có thể nhận biết lọ đựng CH3NH2 bằng cách nào sau đây?
A. Nhận biết bằng mùi.
B. Thêm vài giọt dung dịch H2SO4.
C. Thêm vài giọt dung dịch Na2CO3.
D. Đưa đũa thủy tinh đã nhứng vào dung dịch HCl đậm đặc lên phía trên miệng lọ đựng dung dịch CH3NH2.
Gợi ý đáp án
Đáp án D.
Khi cho CH3NH2 tác dụng với dung dịch HCl đặc ta thấy xung quanh xuất hiện khói trắng. Dựa vào đó nhận biết được CH3NH2.
PTHH: CH3NH2 + HCl → CH3NH3Cl (khói trắng)
Câu 3
Viết công thức cấu tạo, gọi tên và chỉ rõ bậc từng amin có công thức phân tử sau:
a. C3H9N.
b. C7H9N. (có chứa vòng benzen)
Gợi ý đáp án
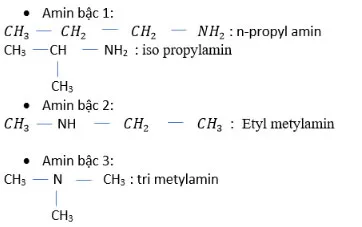
a. C3H9N.
b. C7H9N. (có chứa vòng benzen)
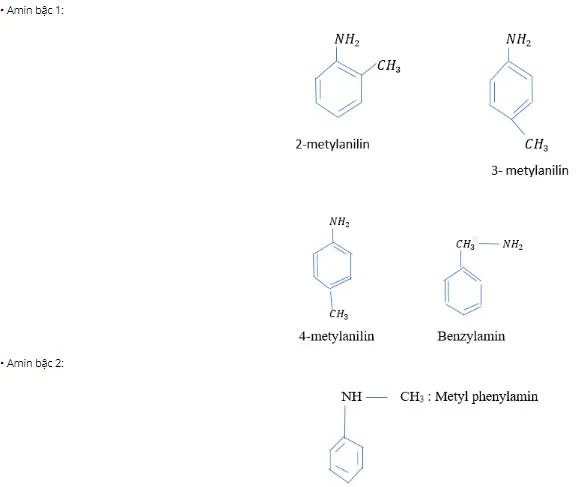
Câu 4
Trình bày phương pháp hóa học hãy tách riêng từng chát trong mỗi hỗn hợp sau đây?
a. Hỗn hợp khí CH4 và CH3NH2.
b. Hỗn hợp lỏng: C6H6, C6H5OH và C6H5NH2.
Gợi ý đáp án
a. Hỗn hợp khí CH4 và CH3NH2
Cho hỗn hợp đi qua dung dịch HCl, CH3NH2 phản ứng với HCl bị giữ lại trong dung dịch, khí thoát ra ngoài là CH4 tinh khiết.
CH3NH2 + HCl → CH3NH2Cl
Cho NaOH vào CH3NH2Cl thu được CH3NH2
CH3NH2Cl + NaOH → CH3NH2 + NaCl + H2O
b. Hỗn hợp lỏng: C6H6, C6H5OH và C6H5NH2
cho dung dịch NaOh vào hỗn hợp lỏng trên thu được dung dịch gồm hai phần: phần tan là C6H5ONa và phần hỗn hợp còn lại là C6H5NH2 và C6H6.
Tách làm hai phần
C6H5OH + NaOH → C6H5ONa + H2O
Sục khí CO2 vào phần dung dịch ta thu được C6H5OH kết tủa .
C6H5ONa + CO2 + H2O → C6H5OH↓ + NaHCO3
Với hỗn hợp cho tác dụng dung dịch HCl, thu dung dịch gồm hai phần : phần tan là C6H5NH3 Cl, phần không tan là C6H6
C6H5NH2 + HCl → C6H5NH3 Cl
Cho dung dịch NaOH vào phần dung dịch, ta thu được C6H5NH2 kết tủa.
C6H5NH3Cl + NaOH → C6H5NH2↓ + NaCl + H2O
Câu 5
Hãy tìm phương pháp hóa học để giải quyết hai vấn đề sau:
a. Rửa lọ đã đựng aniline
b. Khử mùi tanh của cá sau khi mổ để nấu. Biết rằng mùi tanh của cá, đặc biệt là của các mè do hỗn hợp một số amin (nhiều nhát là trimetylamin) và một số tạp chất khác gây nên.
Gợi ý đáp án
a. Rửa lọ đã đựng anilin.
Cho vào lọ đựng anilin dung dịch HCl sau tráng bằng nước cất.
b. Khử mùi tanh của cá, ta cho vào một ít dấm CH3COOH các amin sẽ tạo muối với CH3COOH nên không còn tanh nữa.
(CH3)3N + CH3COOH → CH3COONH(CH3)3
Câu 6
a. Tính thể tích nước brom 3% (D=1,3g/ml) cần để điều chế 4,4 gam tribromanilin.
b. Tính khối lượng anilin có trong dung dịch A biết rằng khi cho tác dụng vào nước brom thì thu được 6,6 gam kết tủa trắng. Giả sử hiệu suất của cả hai trường hợp là 100%.
Gợi ý đáp án
a. Số mol C6H2Br3NH3 là
Theo pt n(Br2) = 3. n(C6H2Br3NH3) = (mol)
Khối lượng Br2 là m(Br2) = . 160 = 6,4 (g)
Khối lượng dung dịch Br2 (3%) là m(ddBr2) = g
Thể tích dung dịch Br2 cần dùng V(ddBr2) = = 164,1 (ml)
b. C6H5NH2 + 3Br2 → C6H2Br3NH2 + 3HBr
số mol kết tủa là n(C6H2Br3NH2) = = 0,02(mol)
theo pt n(C6H5NH2) = n(C6H2Br3NH2) = 0,02 (mol)
khối lượng aniline có trong dung dịch A là m(C6H5NH2) = 93. 0,02 = 1,86(g)