Hoá 9 Bài 46 giúp các em học sinh lớp 9 nắm vững kiến thức về mối liên hệ giữa etilen, rượu etylic và axit axetic. Đồng thời giải nhanh được các bài tập Hóa học 9 chương 5 trang 144.
Bạn đang đọc: Hóa học 9 bài 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic
Việc giải Hóa 9 bài 46 trước khi đến lớp các em nhanh chóng nắm vững kiến thức hôm sau ở trên lớp sẽ học gì, hiểu sơ qua về nội dung học. Đồng thời giúp thầy cô tham khảo, nhanh chóng soạn giáo án cho học sinh của mình. Vậy sau đây là nội dung chi tiết tài liệu, mời các bạn cùng tham khảo tại đây.
Giải Hoá học lớp 9 trang 144
Lý thuyết Mối liên hệ giữa etilen, rượu etylic và axit axetic
Sơ đồ liên hệ giữa etilen, rượu etylic và axit axetic.
Etilen rượu etylic
Axit axetic
Etyl axetat
Phương trình phản ứng minh họa
CH2=CH2 + H-OH CH3-CH2-OH
CH3-CH2-OH + O2 CH3COOH + H2O
CH3COOH + HO-CH2CH3CH3COOC2H5 + H2O
Giải bài tập Hóa 9 Bài 46 trang 144
Câu 1
Chọn các chất thích hợp thay vào chữ cái rồi viết phương trình hóa học theo những sơ đồ chuyển đổi hóa học sau
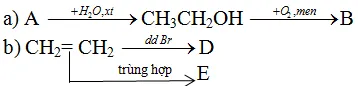
Gợi ý đáp án
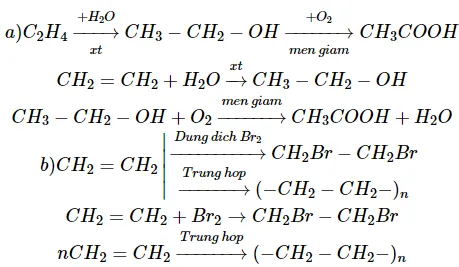
Câu 2
Nêu hai phương pháp hóa học khác nhau để phân biệt hai dung dịch C2H5OH và CH3COOH
Gợi ý đáp án:
Hai phương pháp là:
a) Dùng quỳ tím: Axit axetic làm quỳ tím hóa đỏ Rượu etylic không làm quỳ tím đổi màu
b) Dùng Na2CO3 hoặc CaCO3: CH3COOH cho khí CO2 thoát ra C2H5OH không có phản ứng
CH3COOH cho khí CO2 thoát ra
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
C2H5OH không có phản ứng.
Câu 3
Có ba chất hữu cơ có công thức phân tử là C2H4, C2H4O2, C2H6O được kí hiệu ngẫu nhiên là A, B, C biết
Chất A và C tác dụng được với natri.
Chất B ít tan trong nước.
Chất C tác dụng được với Na2CO3
Hãy xác định công thức phân tử và viết công thức cấu tạo của A, B, C.
Gợi ý đáp án.
Chất C vừa tác dụng với Na, vừa tác dụng với Na2CO3, suy ra trong phân tử có nhóm –COOH.
Vậy C2H4O2 là công thức phân tử của C, công thức cấu tạo của C là: CH3-COOH.
Chất A tác dụng được với Na, suy ra trong phân tử có nhóm –OH. Vậy C2H6O là công thức phân tử của A, công thức cấu tạo của A là C2H5OH.
Chất B không tan trong nước, không phản ứng với Na, Na2CO3 là etilen CH2 = CH2.
Câu 4
Đốt cháy 23 gam chất hữu cơ A thu được sản phẩm gồm 44 gam CO2 và 27 gam H2O
a) Hỏi trong A có những nguyên tố nào
b) Xác định công thức phân tử của A, biết tỉ khối hơi của A so với hidro là 23
Gợi ý đáp án
Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam). Trong A có 3 nguyên tố C, H, O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
=> 46/23 = 12x/12 => x = 2
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O
Câu 5
Cho 22,4 lít khí etilen (ở điều kiện tiêu chuẩn) tác dụng với nước có axit sunfuric làm xúc tác, thu được 13,8 gam rượu etylic. Hãy tính hiệu suất phản ứng cộng nước của etilen.
Gợi ý đáp án
Phản ứng của etylen với H2O:
C2H4 + H2O – H2SO4 → CH3 – CH2OH
Số mol etylen = 22,4/22,4 = 1 (mol)
Theo PTHH, cứ 1 mol etilen khi phản ứng hết với nước tạo ra 1 mol rượu etylic Vậy theo lí thuyết, số mol rượu etylic tạo ra là 1 mol (tính theo etilen vì nước dư) hay 1 x 46 = 46 (gam)
Thực tế lượng rượu thu được là 13,8 gam
Vậy hiệu suất phản ứng là 13,8/46 x 100% = 30%