Giải Hóa 10 Bài 4: Cấu trúc lớp vỏ electron của nguyên tử sách Chân trời sáng tạo là tài liệu vô cùng hữu ích, giúp các em học sinh lớp 10 có thêm nhiều gợi ý tham khảo, nhanh chóng trả lời toàn bộ câu hỏi trong sách giáo khoa trang 26→ 34 thuộc chương 1: Cấu tạo nguyên tử.
Bạn đang đọc: Hóa học 10 Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Hóa 10 bài 4 Cấu trúc lớp vỏ electron của nguyên tử được biên soạn khoa học, chi tiết giúp các em rèn kỹ năng giải Hóa, so sánh đáp án vô cùng thuận tiện từ đó sẽ học tốt môn Hóa học 10. Đồng thời đây cũng là tài liệu giúp quý thầy cô tham khảo để soạn giáo án. Vậy sau đây là giải Hóa 10 bài 4 trang 26 sách Chân trời sáng tạo, mời các bạn cùng theo dõi tại đây.
Giải Hóa 10 Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Giải SGK Hóa 10 Bài 4 trang 34
Bài 1
Trong các cách biểu diễn electron và các orbital của phân lớp 2p ở trạng thái cơ bản, hãy chọn cách phân bố đúng:
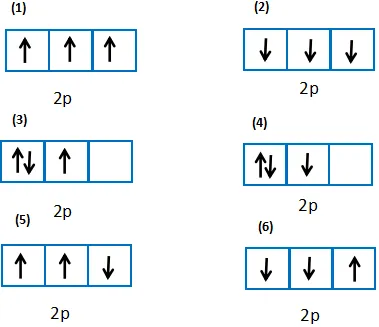
Gợi ý đáp án
(1): đúng vì chứa tối đa electron và biểu diễn electron độc thân bằng mũi tên đi lên
(2): sai vì số electron độc thân chưa tối đa
(3): sai vì biểu diễn 1 electron độc thân bằng mũi tên đi xuống
(4): sai vì biểu diễn electron độc thân bằng mũi tên đi xuống
(5): sai vì số electron độc thân chưa tối đa, biểu diễn electron độc thân bằng mũi tên đi xuống
(6): sai vì biểu diễn 2 electron độc thân bằng mũi tên đi xuống
Bài 2
Cho nguyên tố X có 2 lớp electron, lớp thứ 2 có 6 electron. Xác định số hiệu nguyên tử của X.
Gợi ý đáp án
Lớp thứ nhất có 1 phân lớp là 1s
Lớp thứ 2 có 2 phân lớp là 2s và 2p
Phân lớp s chứa tối đa 2 electron, phân lớp p chứa tối đa 6 electron
=> Cấu hình electron của nguyên tố X: 1s22s22p4
=> Nguyên tố X có 8 electron
=> Số hiệu nguyên tử của X: Z = 8
Bài 3
Ở trạng thái cơ bản, nguyên tử của những nguyên tố nào dưới đây có electron độc thân?
a) Boron
b) Oxygen
c) Phosphorus
d) Chlorine
Gợi ý đáp án
a) Boron (Z = 5): 1s22s22p1 => Có 1 electron độc thân
b) Oxygen (Z = 8): 1s22s22p4 => Có 2 electron độc thân
c) Phosphorus (Z = 15): 1s22s22p63s23p3 => Có 3 electron độc thân
d) Chlorine (Z = 17): 1s22s22p63s23p5 => Có 1 electron độc thân
Bài 4
Viết cấu hình electron nguyên tử của các nguyên tố: carbon (Z = 6), sodium (Z = 11) và oxygen (Z = 8). Cho biết số electron lớp ngoài cùng trong nguyên tử của các nguyên tố trên. Chúng là kim loại, phi kim hay khí hiếm.
Gợi ý đáp án
Nguyên tố Carbon (Z = 6): 1s22s22p2 => Có 4 electron ở lớp ngoài cùng, là nguyên tố phi kim
Nguyên tố Sodium (Z = 11): 1s22s22p63s1 => Có 1 electron ở lớp ngoài cùng, là nguyên tố kim loại
Nguyên tố Oxygen (Z = 8): 1s22s22p4 => Có 6 electron ở lớp ngoài cùng, là nguyên tố phi kim

